
“抗癌神藥”CAR-T療法因安全性問題遭遇監(jiān)管機構(gòu)的調(diào)查。
當?shù)貢r間11月28日,美國食品藥品監(jiān)督管理局(FDA)官網(wǎng)發(fā)布公告稱,將調(diào)查關(guān)于接受靶向BCMA或CD19自體CAR-T 細胞免疫療法治療的患者出現(xiàn)T細胞惡性腫瘤(包括嵌合抗原受體CAR陽性淋巴瘤)的風險,已經(jīng)確認目前批準的所有靶向BCMA和CD19的CAR-T療法都有該風險。簡單來講,F(xiàn)DA認為,接受CAR-T療法的患者有患上其他腫瘤的風險。

FDA在公告中直接點名了4家公司共計6款已在美國獲批的CAR-T療法,包括百時美施貴寶(BMS)的Abecma和Breyanzi,傳奇生物/強生的Carvykti,諾華的Kymriah,吉利德的Tecartus和Yescarta。
或受上述消息影響,除了美股相關(guān)上市公司,港股、A股多家擁有CAR-T療法的上市公司股價也出現(xiàn)不同程度的異動。面對FDA的調(diào)查,多家美國藥企回應稱,還沒有證據(jù)證明CAR-T療法與T細胞惡性腫瘤的關(guān)系。也有港股上市公司強調(diào),這次事件對公司產(chǎn)品的研發(fā)和商業(yè)化進程沒有實質(zhì)影響。
6款產(chǎn)品被點名,F(xiàn)DA調(diào)查攪動全球CAR-T市場
CAR-T療法屬于細胞免疫療法,是在體外利用基因工程的方法修飾患者外周血T細胞,賦予T細胞靶向識別腫瘤細胞表面抗原的特性 ,經(jīng)體外擴增培養(yǎng)后回輸?shù)交颊唧w內(nèi)進行治療腫瘤的方法。簡單來說,CAR-T療法就是利用人體免疫細胞抗癌,有“抗癌神藥”之稱。
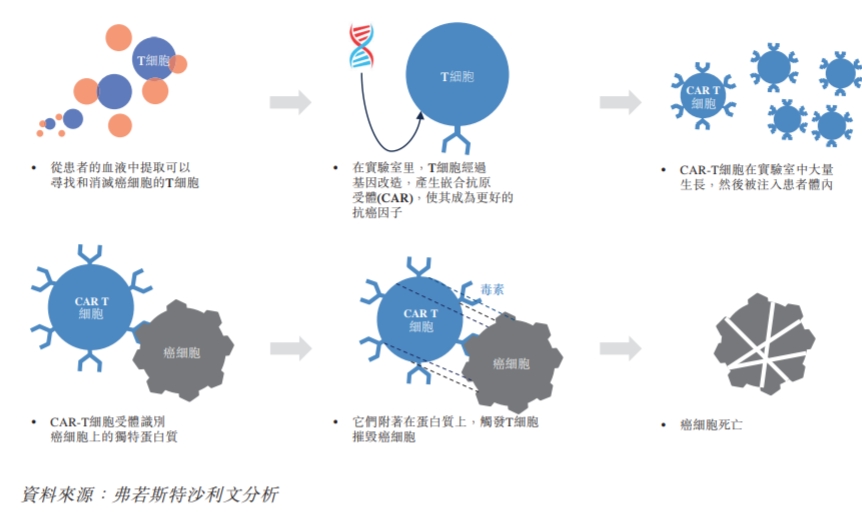
在此次FDA的調(diào)查公告之前,CAR-T療法最受關(guān)注的是其價格,國內(nèi)在百萬級別,國外的價格最高超過45萬美元。此次FDA的調(diào)查則將CAR-T療法的安全性擺在了大眾和行業(yè)面前。根據(jù)FDA的公告,報告的數(shù)據(jù)來自臨床試驗和/或上市后的不良事件。盡管這些產(chǎn)品的總體益處仍超過其批準用途的潛在風險,但FDA正在調(diào)查已確定的風險,這些風險會導致住院和死亡等嚴重后果。
或受上述調(diào)查消息的影響,美股多家擁有CAR-T產(chǎn)品的藥企股價下跌:百時美施貴寶(BMY) 28日和29日均小幅收跌;吉利德科學(GILD)和諾華(NVS)28日均收跌,29日小幅收漲;傳奇生物(LEGN)28日收跌2.55%,29日收跌0.28%。
傳奇生物的CAR-T療法是為數(shù)不多在美國獲批的國產(chǎn)創(chuàng)新藥,其出海方式是牽手知名跨國企業(yè)強生,目前該產(chǎn)品還未在國內(nèi)獲批。不過,傳奇的母公司是港股上市公司金斯瑞生物科技(1548.HK),金斯瑞生物科技29日收跌6.02%,30日盤中跌幅一度超5%,收跌0.23%。
目前,國內(nèi)已經(jīng)獲批的CAR-T療法共有四款,其中包括復星醫(yī)藥(600196.SH;2196.HK)和藥明巨諾(02126.HK)兩家上市公司。
復星醫(yī)藥的阿基侖賽注射液是中國首個獲批上市的CAR-T產(chǎn)品,是復星凱特從美國Kite Pharma(吉利德科學旗下公司)引進Yescarta技術(shù),同時獲得授權(quán)在中國進行本地化生產(chǎn)的靶向CD19自體CAR-T療法,Yescarta此次也被FDA點名。復星醫(yī)藥29日A股收跌1.35%,港股收跌3.24%,30日港股收跌1.38%。
藥明巨諾的瑞基奧侖賽注射液是國內(nèi)獲批的第二款CAR-T產(chǎn)品。11月28日,CDE 官網(wǎng)顯示,擬將瑞基奧侖賽注射液納入優(yōu)先審評,用于治療成人復發(fā)或難治性套細胞淋巴瘤。積極進展遭遇美國的調(diào)查風波,藥明巨諾29日平收,30日微漲0.61%。
除了已經(jīng)獲批的CAR-T療法背后的上市公司,此次調(diào)查風波也波及到在研CAR-T療法的上市公司。以科濟藥業(yè)(02171.HK)為例,該公司專注于治療血液惡性腫瘤和實體瘤的創(chuàng)新CAR-T細胞療法,旗下CAR-T產(chǎn)品澤沃基奧侖賽注射液的上市申請于2022年10月獲得受理,預期將于2023年底或2024年初獲批用于治療復發(fā)/難治多發(fā)性骨髓瘤。FDA的調(diào)查公告宣布后的29日,科濟藥業(yè)大跌23.29%。
多家企業(yè)回應:對公司CAR-T產(chǎn)品的安全性充滿信心
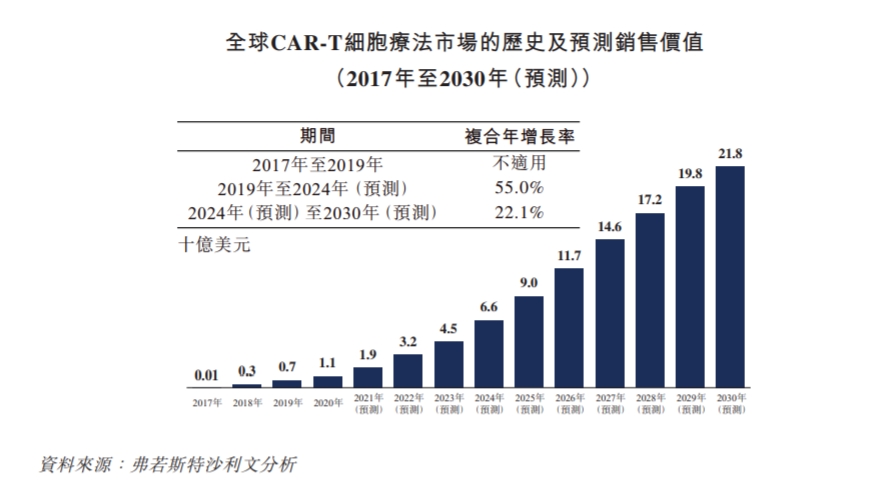
據(jù)弗若斯特沙利文數(shù)據(jù),按銷售價值計算,全球CAR-T市場規(guī)模從2017年的0.1億美元增長到2019年的7億美元,預計到2030年全球CAR-T市場規(guī)模預計達到218億美元,2024年至2030年的復合年增長率為22.1%。
CAR-T賽道吸引了眾多玩家,不僅包括強生、諾華等成熟的跨國藥企,也包括傳奇生物、科濟藥業(yè)等新興的生物科技公司,有產(chǎn)品已經(jīng)成為企業(yè)的重磅產(chǎn)品。以2022年為例,全球CAR-T市場規(guī)模接近27億美元,其中吉利德的Yescarta全年營收11.6億美元,成為首款年銷售額超過10億美元的CAR-T療法。
面對FDA給CAR-T賽道潑的這盆冷水,眾多公司紛紛作出回應,大都強調(diào),公司對自家CAR-T療法的安全性充滿信心,且目前證據(jù)尚無法說明該產(chǎn)品與繼發(fā)性腫瘤的因果關(guān)系。
吉利德方面表示,將完全配合FDA的要求,對CAR-T療法的數(shù)據(jù)進行額外分析,公司對兩款CAR-T療法的整體安全性充滿信心,已有17700名患者在臨床試驗和商業(yè)環(huán)境中接受了這些產(chǎn)品的治療。目前為止,還沒有證據(jù)表明接受兩款產(chǎn)品治療與新繼發(fā)性惡性腫瘤的發(fā)生有因果關(guān)系。
對于Kymriah的安全性,諾華表示,在治療了1萬多名患者后,該公司尚未確定CAR-T產(chǎn)品與繼發(fā)性惡性腫瘤之間的因果關(guān)系。值得關(guān)注的是,除了Kymriah,11月13日,諾華制藥還曾宣布,與傳奇生物就傳奇生物的特定靶向DLL3的嵌合抗原受體T細胞(CAR-T)療法簽訂獨家全球許可協(xié)議,協(xié)議授予諾華開發(fā)、制造和商業(yè)化這些細胞療法的全球獨家權(quán)利,該協(xié)議的總交易金額達到11.1億美元。
面對FDA對Carvykti的安全性調(diào)查,傳奇生物公開回應稱,即使沒有進行CAR-T細胞治療,多發(fā)性骨髓瘤患者也可能發(fā)生T細胞惡性腫瘤。此外,其他與骨髓瘤相關(guān)的治療,例如烷基化劑、免疫調(diào)節(jié)藥物和自體干細胞移植,都與繼發(fā)性癌癥的風險增加有關(guān)。傳奇生物的合作伙伴美國強生公司也在表示,已與FDA共享Carvykti治療后的監(jiān)測數(shù)據(jù),Carvykti迄今已在2000名患者身上使用,具有良好的收益風險比。
擁有兩款CAR-T療法的BMS也在聲明中強調(diào),對公司的細胞療法的安全性和臨床價值保持信心,公司已經(jīng)在臨床和商業(yè)環(huán)境中為超過4700名患者使用兩款產(chǎn)品治療,目前尚未觀察到任何CAR陽性T細胞惡性腫瘤病例,因此我們未發(fā)現(xiàn)我們的產(chǎn)品與繼發(fā)性惡性腫瘤之間存在因果關(guān)系。
對于FDA的調(diào)查,國內(nèi)CART-療法相關(guān)公司大多未對外發(fā)聲。11月30日早間,科濟藥業(yè)發(fā)布聲明表示,基于目前已經(jīng)公開發(fā)表的信息,T細胞惡性腫瘤在接受CAR-T治療患者中的發(fā)病率非常低。截至目前,科濟藥業(yè)在研CAR-T產(chǎn)品,臨床試驗治療患者總數(shù)超過500例,其中靶向BCMA CAR-T產(chǎn)品250余例,未觀察到T細胞腫瘤案例。這次事件對公司產(chǎn)品的研發(fā)和商業(yè)化進程沒有實質(zhì)影響。
11月30日,科濟藥業(yè)創(chuàng)始人、董事會主席、首席執(zhí)行官、首席科學官李宗海在接受澎湃新聞記者采訪時表示,F(xiàn)DA對CAR-T產(chǎn)品展開調(diào)查是出于對公眾負責的態(tài)度,但最終還是需要做大量數(shù)據(jù)的采集分析,用數(shù)據(jù)說話,“最終還是回到數(shù)據(jù)上,這個藥好不好,獲益風險比是怎樣的”。至少目前在血液腫瘤領(lǐng)域,CAR-T展示了非常強大的療效和很好的獲益風險比,這也是為什么CAR-T療法受歡迎的重要原因。
科濟藥業(yè)在聲明中援引Moffitt癌癥中心的Frederick Locke教授在MedPage Today的觀點提到,“接受CAR-T治療的患者中,T細胞淋巴瘤的發(fā)生率約為萬分之一或二”。李宗海向澎湃新聞記者介紹,現(xiàn)在圍繞CAR-T的另一個研究方向是自身免疫性疾病,這類患者本身沒有腫瘤,且是慢性病,哪怕有萬分之幾的可能致癌,也會受到更大關(guān)注。盡管如此,最終也要看獲益風險比,至少CAR-T已看到在自免疾病治療,如系統(tǒng)性紅斑狼瘡的良好前景,只是在慢病領(lǐng)域需要更長時間的觀察和理解這種獲益風險比。FDA此次的調(diào)查對做自身免疫性疾病的CAR-T公司可能沖擊更大一些,對做腫瘤適應證的公司影響相對較小。
對于此次調(diào)查對整個CAR-T行業(yè)的影響,李宗海認為,短期有一定影響,但長期來看,行業(yè)的前景還是取決于CAR-T本身的安全性和有效性。目前還沒有明確的證據(jù)證明CAR-T產(chǎn)品和繼發(fā)性腫瘤之間的因果聯(lián)系。此外,CAR-T的技術(shù)發(fā)展空間很大,將來還可以通過技術(shù)進一步改造提高產(chǎn)品的安全性,這也是企業(yè)可以做的方向。

 京公網(wǎng)安備 11010802028547號
京公網(wǎng)安備 11010802028547號