
5月31日,康方AK112的HARMONi-2研究結(jié)果發(fā)布,稱其在頭對頭試驗中擊敗了K藥,顯著提高了患者的無進(jìn)展生存期(PFS),超預(yù)期改善了風(fēng)險比(HR)。
但在默沙東EliavBarr博士接受FiercePharma采訪時看來,其成功雖不可否認(rèn),但需要后續(xù)更多OS數(shù)據(jù)的進(jìn)一步證實,畢竟就有效性而言,如“可樂療法”等多種治療方案在過去也曾取得過更優(yōu)秀的疾病進(jìn)展或更低的死亡風(fēng)險,后續(xù)卻都折戟于總生存期指數(shù)上(可樂療法有10%的負(fù)面趨勢)。
加之,如今FDA對于創(chuàng)新藥療法的OS指數(shù)愈發(fā)看重,AK112要想在一線NSCLC中獲得FDA的批準(zhǔn),基于以往PD-1/VEGF組合的經(jīng)驗,這可能是一個挑戰(zhàn),言外之意似乎是說,AK112要想在OS數(shù)據(jù)上擊敗K藥似乎難度不小。
如此,考慮到目前創(chuàng)新藥出海的整體局勢,或許OS還將是AK112繞不開的坎,更是中國創(chuàng)新藥繞不開的坎。
FDA對OS的要求日益嚴(yán)格
多年以來,F(xiàn)DA一直都是將PFS作為抗癌療法獲批的最主要指標(biāo),而在這項舉措之下,全球創(chuàng)新藥的獲批速度確實也得到大幅提升,大批創(chuàng)新藥得以順利上市。然而隨著當(dāng)下越來越多抗癌創(chuàng)新療法的誕生,創(chuàng)新藥企也被FDA要求提供更充分的證據(jù),證實療法對延長患者生存期的實質(zhì)性作用,言外之意就是臨床試驗中更金標(biāo)準(zhǔn)的“OS數(shù)據(jù)”。
畢竟,無論是臨床最終受益、藥物經(jīng)濟(jì)學(xué)、還是創(chuàng)新藥的最終歸屬,患者,尤其是晚期腫瘤患者對抗癌治療的需求都圍繞著“能活多久”。FDA強調(diào)更可靠OS數(shù)據(jù)的要求,顯示了其致力于確保新的抗癌藥物不僅要有延緩疾病進(jìn)展的效果,同時也要在提高患者整體生存期和生活質(zhì)量方面有所作為。
2020年6月,F(xiàn)DA加速批準(zhǔn)了Lurbinectedin(Zepzelca)的上市需求,使其成為自1996年以來首個FDA批準(zhǔn)用于SCLC二線治療的新藥。其審批主要基于單臂試驗數(shù)據(jù),彼時治療組與化療組對比并無顯著的OS差異。
2022年2月10月,F(xiàn)DA拒絕批準(zhǔn)了信達(dá)PD-1,要求其補充臨床試驗,除了多地區(qū)數(shù)據(jù)、頭對頭等要求外。也要求信達(dá)應(yīng)以總生存期(OS)為終點。
2023年12月26日,F(xiàn)DA拒絕了安進(jìn)KRASG12C抑制劑Sotorasib從加速批準(zhǔn)轉(zhuǎn)為完全批準(zhǔn)的請求,其原因是Sotorasib相較于多西他賽,雖然PFS有改善,但是OS并沒有明顯提高。
三個時間段,分別是FDA對于創(chuàng)新藥上市申請數(shù)據(jù)的不同態(tài)度,F(xiàn)DA對于OS的要求正在愈發(fā)嚴(yán)格。
PFS的時代正在過去
PFS能被作為OS的替代指標(biāo),原因之一在于,其使臨床試驗?zāi)茉诟虝r間內(nèi)完成,且所需的樣本量更小,更快地證實臨床效益。當(dāng)然,從患者角度來看,PFS也確實是一種“時效性”更強的指標(biāo),大多數(shù)情況下,PFS提升之下,即使OS并無提升,對于臨床上患者的“生活質(zhì)量”的改善也有著顯著改善,在整個治療過程中也顯得尤為重要。
但是,PFS與OS之間的正向相關(guān)性卻也并非絕對,其往往會因為多種原因而發(fā)生顛覆性變化,比如部分創(chuàng)新藥療法雖然早期PFS數(shù)據(jù)優(yōu)秀,但較大的副作用反而會對總生存期與生活質(zhì)量產(chǎn)生反向影響。
FDA腫瘤卓越中心主任RichardPazdur博士在去年7月份舉行的FDA-AACR行業(yè)聯(lián)合研討會上解釋說,PFS終點的長期使用是在細(xì)胞毒性化療成為常規(guī)療法的情況下產(chǎn)生的,在此情形下,緩解率、疾病進(jìn)展和生存期之間存在很強的相關(guān)性。然而,當(dāng)使用新型藥物進(jìn)行治療時,這種情況可能并不總是正確的。
另外,PFS某種程度上還存在一定的主觀性,在alex研究中,研究者與獨立審評委員會的治療評估PFS上就存在9.1個月的差距;同時,PFS對于免疫治療而言也呈現(xiàn)較明顯的局限性,有關(guān)研究中顯示,免疫治療與多西他賽相比,雖未達(dá)到延長PFS的場景,但OS獲益明顯,這就是表示免疫治療存在假進(jìn)展或延遲效應(yīng),表明PFS在評估免疫治療的療效上存在滯后性。
FDA在《LancetOncology》上發(fā)布的一項匯總分析探究了ICI一線治療NSCLC時帶來的ORR和PFS獲益與總生存期(OS)的關(guān)系。結(jié)果顯示,在PD-L1>1%的患者里,無論是ORR還是PFS,對OS的預(yù)測都落在弱相關(guān)區(qū)域,尤其是PD-L1≥50%的患者,ORR對OS的預(yù)測處于極弱相關(guān)。這意味著,在該階段用ORR或PFS預(yù)測該類患者的OS幾乎是一個隨機(jī)事件。
綜上所述,隨著免疫治療時代的到來,過去以PFS為主要終點的審批模式或許某種程度已不再完全適用,創(chuàng)新藥的PFS時代正在過去,創(chuàng)新藥企或許需要將更多重心放在OS數(shù)據(jù)上。
國產(chǎn)創(chuàng)新藥出海,OS是繞不開的坎
以目前FDA對于OS的硬性態(tài)度來看,對于國內(nèi)創(chuàng)新藥出海,其在未來極可能會因為OS試驗的復(fù)雜性而極大地延長藥物獲批周期,使研發(fā)的時間與成本大幅上漲。
數(shù)據(jù)收集難度大:相比PFS數(shù)據(jù)的收集,收集和分析OS數(shù)據(jù)往往更為復(fù)雜和耗時,需要較長的隨訪時間和更大的樣本量。
數(shù)據(jù)解讀難度大:OS干擾因素繁雜,不同試驗不同群體都可能導(dǎo)致OS數(shù)據(jù)不夠準(zhǔn)確,解讀困難大。
存在倫理考量:由于現(xiàn)有治療并不能保證生存周期內(nèi)單用研究藥物,故隨訪過程中也許存在交叉治療的影響,最終導(dǎo)致OS數(shù)據(jù)不可信。
而對于近年來FDA對于臨床數(shù)據(jù)的態(tài)度改變,有了之前信達(dá)PD-1的前車之鑒,中國不少創(chuàng)新療法對于OS數(shù)據(jù)的前瞻布局也在順利推進(jìn)。近日召開的ASCO大會上,已有部分的創(chuàng)新療法公布了最新的OS數(shù)據(jù)。
ASCO大會上部分國產(chǎn)新藥的PFS與OS數(shù)據(jù)
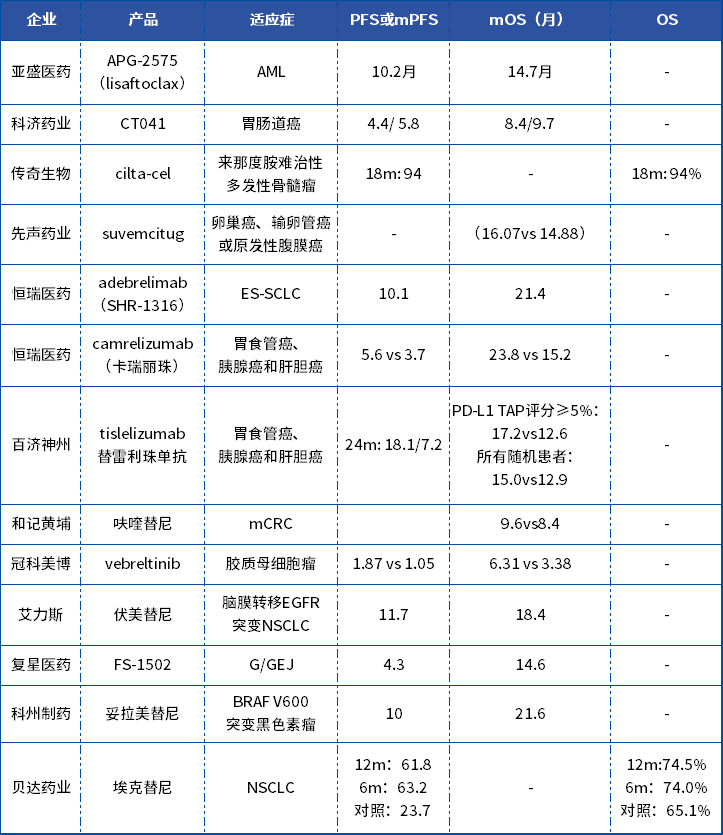
數(shù)據(jù)來源:2024ASCO大會
以恒瑞卡瑞利珠單抗為例,借ASCO大會的契機(jī),ESCORT-1st研究的數(shù)據(jù)振奮人心,在聯(lián)合化療一線治療晚期ESCC上,不僅取得了7.6個月的中位PFS數(shù)據(jù),同時在“生存期數(shù)據(jù)”上尤為重視,多項相關(guān)數(shù)據(jù)作為重點披露:
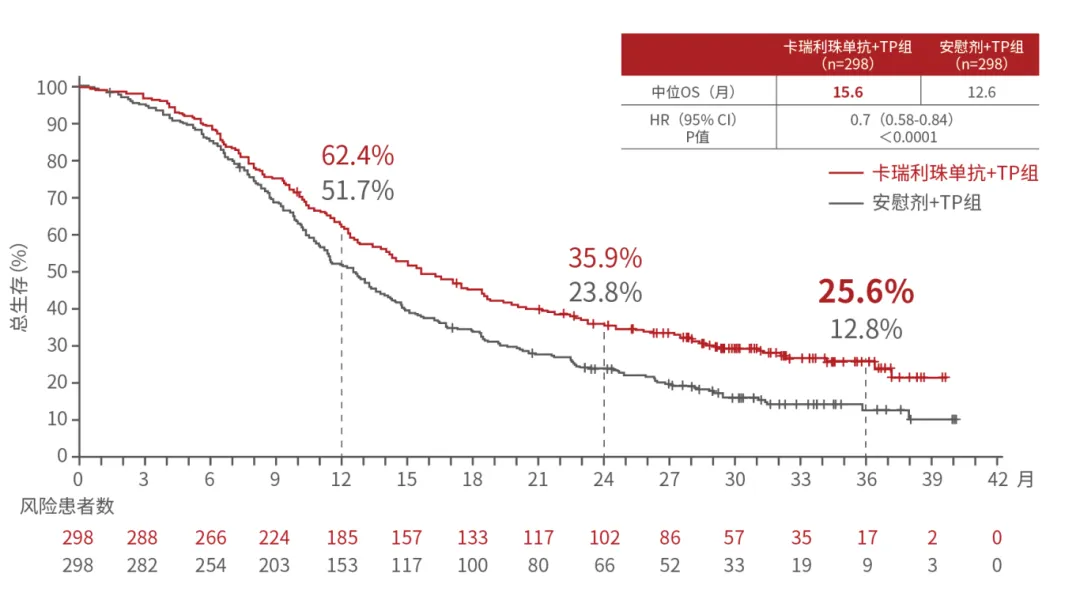
圖3:ESCORT-1st研究亞組生存曲線
圖片來源:醫(yī)脈通腫瘤科
中位總生存期(OS):15.6個月;
3年總生存率:25.6%(刷新現(xiàn)有一線免疫聯(lián)合化
PD-L1TPS<1%的3年生存率:從14.2%提升到24.4%;
PD-L1TPS≥1%的3年生存率:從11.4%躍升至25.9%;
小結(jié)
顯然,無論是從審批機(jī)構(gòu)透露的指導(dǎo)意見,還是創(chuàng)新藥企的臨床試驗計劃,亦或是披露數(shù)據(jù)的重點上,均可看出目前創(chuàng)新藥研發(fā)以O(shè)S為新重點的趨勢。
并且,隨著靶向抗癌藥的持續(xù)普及,這個趨勢還將延續(xù),新藥上市或許也將由快速時代進(jìn)入慢時代
轉(zhuǎn)載來源:藥智頭條

 京公網(wǎng)安備 11010802028547號
京公網(wǎng)安備 11010802028547號