
3月14日,康希諾發(fā)布公告,收到巴西法院送達(dá)的Belcher向其提起訴訟的請愿書、立案通知等相關(guān)材料。Belcher請求判令康希諾向Belcher支付收益損失和精神損害賠償共計約1.67億雷亞爾(約合人民幣2.41億元)。截至目前,該案件尚未開庭審理。

圖片來源:康希諾官網(wǎng)
事件的起因是,2021年康希諾擬向巴西國家衛(wèi)生監(jiān)督局(ANVISA)遞交重組新型冠狀病毒疫苗(5型腺病毒載體)緊急使用許可的申請,為此,公司于2021年4月19日向Belcher出具了“LETTER OF AUTHORIZATION” (以下簡稱“《授權(quán)函》” ),授權(quán)Belcher代表公司與當(dāng)?shù)卣畽C構(gòu)就新冠疫苗在巴西注冊和商業(yè)化進(jìn)行必要的協(xié)商洽談,有效期6個月(除非公司提前撤銷該授權(quán))。但由于康希諾的新冠疫苗沒有在巴西獲得緊急使用許可,所以康希諾于2021年6月10日向Belcher發(fā)送了“NOTICE OF REVOCATION OF LETTEROF AUTHORIZATION” (以下簡稱“《撤銷授權(quán)函的通知》” )。截至現(xiàn)在,康希諾的新冠疫苗都未在巴西獲得緊急使用許可。
簡單來說,康希諾為了在巴西銷售新冠疫苗向Belcher授權(quán),但是后來新冠疫苗沒有通過巴西的緊急使用許可,所以解除了對Belcher的授權(quán)。但現(xiàn)在,Belcher要求康希諾賠償其2.41億元的收益損失和精神損失費。
不過康希諾認(rèn)為,公司已經(jīng)撤銷對Belcher的授權(quán),且未曾與Belcher簽署過其他任何書面協(xié)議,公司具有較強的抗辯立場,該訴訟案件不會對公司日常生產(chǎn)經(jīng)營產(chǎn)生重大影響。
但是康希諾真正的煩惱或許來自其業(yè)績。
高速墜落的新冠疫苗
不久前,康希諾公布2023年度業(yè)績預(yù)告,全年營收3.57億元,同比減少65.49%;歸母凈利潤-14.47億元,同比虧損增加59.14%。而在兩年前的2021年,康希諾營收達(dá)到近43億元,同比增長17174%;凈利潤19.14億元,同比增長582.65%。
在投資市場,康希諾A股的股價一度漲到797元/股,市值接近2000億元。但截至2024年3月15日收盤,康希諾總市值僅剩138.9億,較高點跌去了九成。
當(dāng)然,其他新冠疫苗相關(guān)企業(yè)與康希諾也有相似經(jīng)歷,業(yè)績在這幾年大起大落。
跨國制藥巨頭輝瑞2023年營收同比下降41%至584.96億美元;凈利同比下降93%至21.19億美元。
Moderna 2023營收68.48億美元,同比下降64.45%;凈利潤-47.14億美元,同比下降156.37%。
BioNtech 2023前三季度總收入為8.95億歐元,相比下降了74%。
表1. 全球新冠相關(guān)產(chǎn)品銷售情況
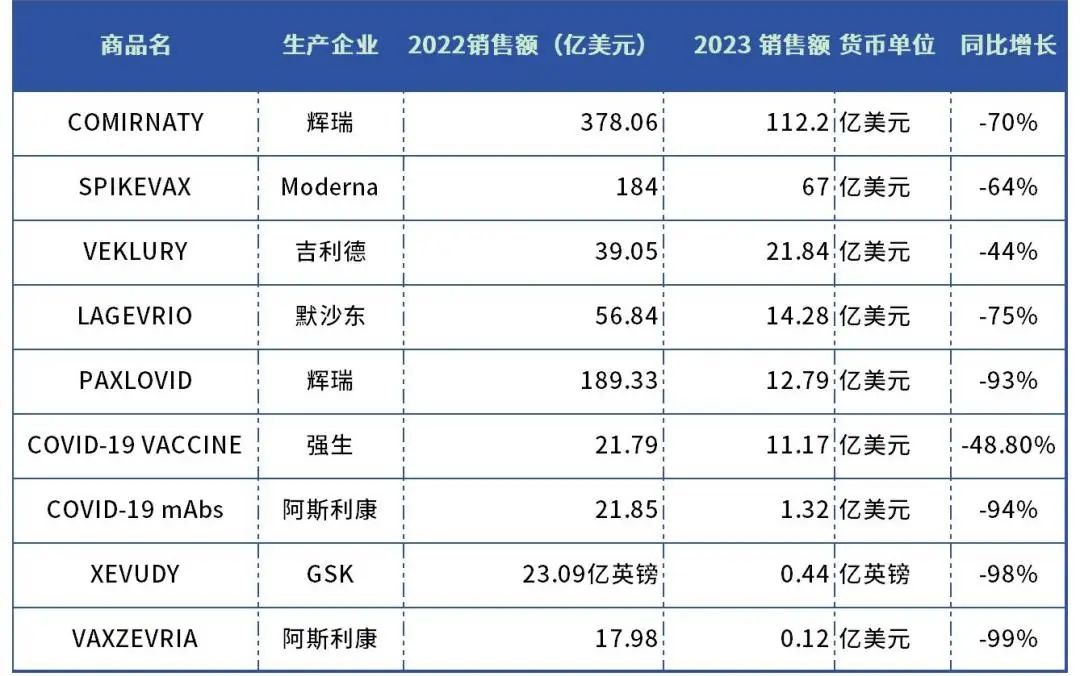
資料來源:根據(jù)企業(yè)公開信息整理
隨著疫情進(jìn)入新的階段,曾因新冠相關(guān)產(chǎn)品而獲益頗多的企業(yè)不得不尋求轉(zhuǎn)型之路。
在全球,Moderna重金投入開發(fā)其他mRNA疫苗;BioNtech從中國數(shù)次引進(jìn)腫瘤管線,重回免疫腫瘤賽道。
康希諾一方面,在去年4月暫停了子公司上藥康希諾生產(chǎn)線,今年2月,康希諾發(fā)布公告,宣布不再將子公司上藥康希諾納入合并報表范圍。另一方面重新回歸創(chuàng)新疫苗研發(fā)專業(yè),大力推進(jìn)多種疫苗的研發(fā)。
多種疫苗已進(jìn)入臨床階段
康希諾官網(wǎng)顯示,目前已有5個上市產(chǎn)品包括:2個新型冠狀病毒疫苗、四價流腦結(jié)合疫苗(商品名:曼海欣)、二價流腦結(jié)合疫苗(商品名:美奈喜)和埃博拉病毒病疫苗。
公司擁有五大技術(shù)平臺,包括病毒載體疫苗技術(shù)、合成疫苗技術(shù)、蛋白結(jié)構(gòu)設(shè)計和VLP組裝技術(shù)、mRNA疫苗技術(shù)、制劑及給藥技術(shù)。除了已上市的產(chǎn)業(yè),還有多個疫苗已進(jìn)入臨床階段,涵蓋對結(jié)核病、腦膜炎、百日咳、白喉、破傷風(fēng)、帶狀皰疹等一系列疾病的預(yù)防。
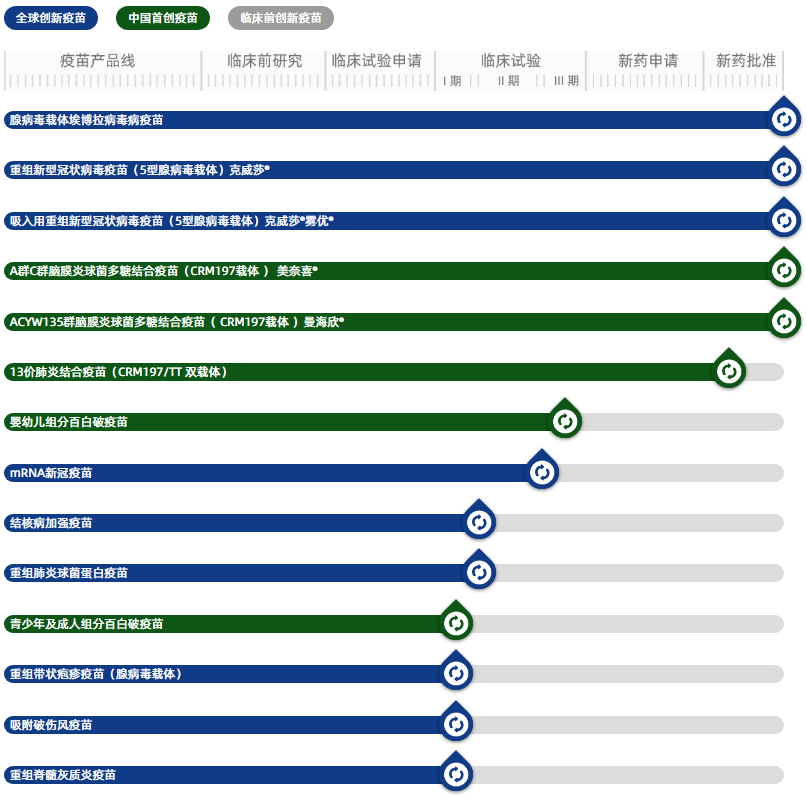
圖片來源:康希諾官網(wǎng)
曼海欣是中國首款自研國產(chǎn)四價流腦多糖結(jié)合疫苗,用于預(yù)防兒童因A群、C群、W135群和Y群腦膜炎奈瑟球菌引起的流行性腦脊髓膜炎。目前來看,該疫苗是康希諾繼新冠疫苗后首個支柱產(chǎn)品。
該疫苗是國內(nèi)唯一可用于3月齡~3周歲(47月)齡兒童接種的四價流腦多糖結(jié)合疫苗。同時,康希諾已經(jīng)在對其四價流腦疫苗作擴齡和出海準(zhǔn)備。針對4-6周歲的研究已經(jīng)進(jìn)入臨床試驗階段,針對7-59歲人群也已獲得臨床試驗批準(zhǔn)。康希諾還與沙特阿拉伯藥品制造公司SPIMACO簽署疫苗合作框架協(xié)議,擬將四價流腦結(jié)合疫苗進(jìn)入沙特阿拉伯以及其他中東和北非地區(qū)市場。
康希諾另一個備受關(guān)注的疫苗——13價肺炎球菌多糖結(jié)合疫苗(CRM197,TT載體,簡稱PCV13i),也已于2024年2月申報上市并獲CDE受理。肺炎球菌性疾病是全球嚴(yán)重的公共衛(wèi)生問題之一,目前國內(nèi)僅輝瑞沛兒13、沃森的沃安欣和民海生物的維民菲寶上市。康希諾生物的PCV13i采用多糖抗原與蛋白載體共價結(jié)合的方式,多糖抗原連接載體蛋白后,多糖可以轉(zhuǎn)化為T細(xì)胞依賴性抗原,不僅可以在2歲以下嬰幼兒體內(nèi)誘導(dǎo)出很高的特異性抗體水平,還可以產(chǎn)生記憶性B細(xì)胞,產(chǎn)生免疫記憶。
此外,自2023年下半年以來,康希諾已將多個疫苗推進(jìn)至臨床階段,包括重組帶狀皰疹疫苗(腺病毒載體)、吸附無細(xì)胞百(組分)白破聯(lián)合疫苗、吸附破傷風(fēng)疫苗、重組脊髓灰質(zhì)炎疫苗等。
小 結(jié)
2017年,康希諾的埃博拉疫苗獲批上市,成為全球第三,亞洲首個埃博拉疫苗,康希諾首次贏得關(guān)注。
2021年,康希諾的新冠疫苗成功上市銷售,成為我國首個被批準(zhǔn)上市的腺病毒載體新冠疫苗,同時該疫苗還獲得了墨西哥、巴基斯坦等多個國家的緊急使用授權(quán)。康希諾再獲關(guān)注。
近日世界衛(wèi)生組織總干事譚德塞就“X疾病”暴發(fā)的可能性發(fā)出公開警告。所謂“X疾病”,并不代表某一種具體的疾病,而是一種由未知病原體引發(fā)、可能導(dǎo)致全球大流行的傳染病。“X疾病”最主要的特點是“高致命、傳染快、易變異”,例如COVID-19就是一種“X疾病”。
各國專家普遍認(rèn)為,受全球氣候加速變化、人類活動范圍不斷擴大、病原跨物種傳播頻繁發(fā)生等因素影響,由“X疾病”引發(fā)全球大流行的風(fēng)險在持續(xù)增加。
雖然現(xiàn)階段新冠病毒疫情已進(jìn)入新階段,但康希諾對傳染性疾病的理解和疫苗開發(fā)經(jīng)驗將助力公司走向更遠(yuǎn)。
轉(zhuǎn)載來源:藥智網(wǎng) 作者:游游

 京公網(wǎng)安備 11010802028547號
京公網(wǎng)安備 11010802028547號